.

تبدیل نوشته به PDF با استفاده از خود برنامه ورد (Word)
اگر برنامه ورد از مجموعه Office را داشته باشید، تبدیل نوشتهها به PDF کاری نخواهد داشت. کافیست:
۱- برنامه ورد را باز کرده و نوشته خود را بارگذاری کنید.
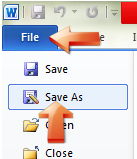
۲- کلید F12 را زده یا به منوی ورد (دکمه File یا آیکون آفیس) رفته و روی Save As کلیک کنید.
۳- در پنجره باز شده و قسمت Save as type گزینه PDF را انتخاب کنید.
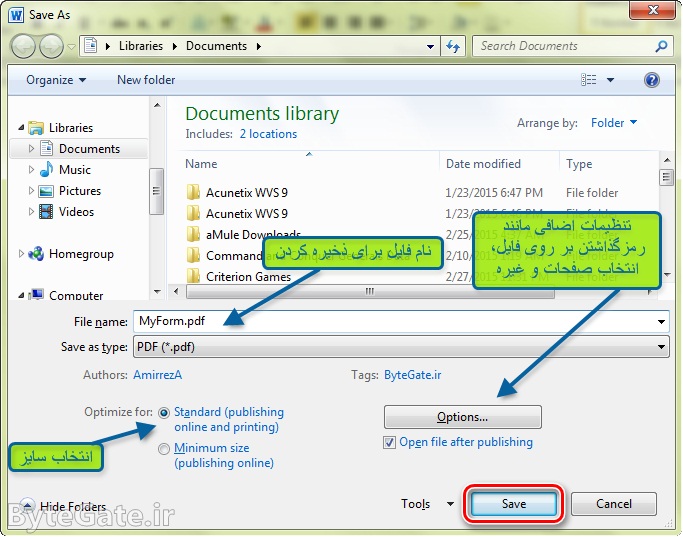
۴- حال نام فایل PDF ومحل ذخیره آن را انتخاب کنید. در قسمت Optimize for سایز استاندارد را انتخاب کرده و برای گزینههای اختیاری از جمله رمزگذاری کردن فایل، انتخاب صفحات و ... روی Options کلیک کنید. در نهایت برای تبدیل و ذخیره کردن روی Save کلیک کنید.
تبدیل نوشته به PDF با برنامه Nemo Word to PDF
اگر برنامه ورد از مجموعه آفیس را در اختیار نداشته باشید، باید از برنامههای جانبی برای تبدیل نوشتهها استفاده کنید. یکی از بهترین این برنامهها Nemo است.
۱- برنامه Nemo Word to PDF را دانلود کرده و نصب کنید. لینک دانلود
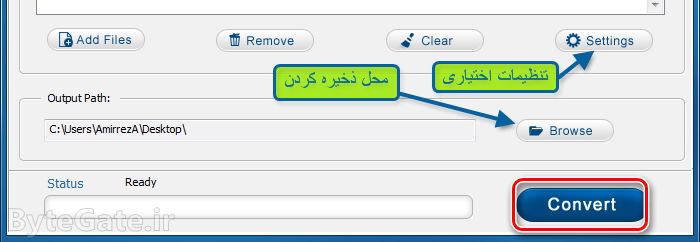
۲- برنامه را باز کرده و روی Add files کلیک کنید. حال فایل(های) ورد خود را انتخاب کنید.
۳- برای تنظیم کردن محل ذخیره فایل PDF کافیست روی Browse کلیک کنید. دکمه Settings هم تعدادی از تنظیمات اختیاری را در اختیار شما قرار میدهد. در نهایت برای تبدیل فایل روی Convert کلیک کنید.
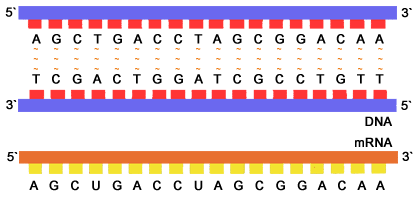
در هسته هر سلول مولکولهایی قرار دارند که اساسی ترین اطلاعات حیات را در خود ذخیره کرده اند. این مولکول ها، دئوکسی ریبو نوکلئیک اسید (DNA) نام دارند. DNA از چهار نوع مولکول ساخته شده است، که به آنها " نوکلئوتید " می گوییم. این چهار نوکلئوتید عبارتند از: ادنین (A)، گوانین (G)، سیتوزین (C) و تیمین (T). این مولکولها خود به دو زیر گروه تقسیم می شوند: ادنین و گوانین در گروه پیورین قرار می گیرند و سیتوزین و تیمین در گروه پیریمیدین جای داده می شوند. هنگام سنتز (ساخته شدن) مولکول DNA، نوکلئوتیدها به اسیدهای نوکلئیک تبدیل می شوند که بعدا به هم متصل می شوند و رشته های DNA را می سازند. در نهایت یک مارپیچ دوتایی ساخته می شود.
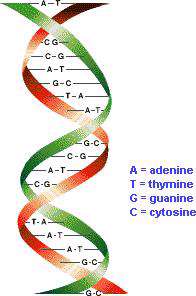
نوکلئوتیدها حلقه های مسطحی دارند که اندازه آنها بین 3 تا 4 آنگستروم ( هر آنگستروم 10-10 متر است.) می باشد. وقتی مارپیچ دوتایی تشکیل می شود، مولکولهای A با مولکولهای T رشته مقابل و مولکول G با مولکول C رشته روبه رو پیوند هیدروژنی برقرار می کنند و جفت های قلیایی ایجاد می شود. این جفت های قلیایی باعث می شوند که مارپیچ پایدار باقی بماند. تصاویری که با استفاده از اشعه X از مولکول DNA گرفته شده است، نشان می دهد که در هر دور از مارپیچ 10 جفت قلیایی وجود دارد.
مدل مارپیچی می تواند نحوه رونویسی از مولکول DNA در هنگام تقسیم سلول را نیز توجیه کند. جیمز واتسون وقتی این مدل را ارائه کرد، آن را " مدل خوش نما " نامید، چون معتقد بود که هر کس این مدل را ببیند می تواند به راحتی نحوه رونویسی از آن را نیز بفهمد. در هنگام تقسیم سلول، باید نسخه مشابهی از DNA تهیه شود تا در سلولهای جدید قرار گیرد. این فرآیند اصطلاحا "رونویسی" نامیده می شوند.
برای انجام این کار، اتصالات هیدروژنی بین نوکلئوتیدها باز می شود و در نتیجه دو رشته مارپیچ از هم باز می شوند. سپس هر یک از این رشته ها به عنوان پایه ای برای ساخت رشته مقابل استفاده می شود. به این ترتیب دو مارپیچ کاملا یکسان DNA ساخته می شوند و هر کدام از آنها در یکی از دو سلول نوزاد قرار می گیرد. چون در هر بار رونویسی، نیمی از مولکول DNA قبلی حفظ می شود، می گوییم رونویسی DNA، نیمه پایستار است.
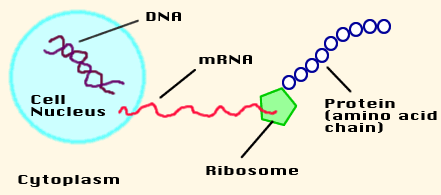
اگرچه DNA اطلاعات ژنتیکی جاندار زنده را در خود دارد، اما برای عملکرد موفق به وجود ریبونوکلئیک اسید (RNA) نیاز دارد. RNA هم مانند DNA از رشته های اسید نوکلئیکی تشکیل شده که با پیوندهای مشابهی به هم متصل شده اند؛ اما دو تفاوت عمده با DNA دارد. یکی اینکه در ساختار آن به جای تیمین، از اوراسیل(u) استفاده شده است و دوم اینکه مارپیچی نیست و فقط از یک رشته تنها ساخته شده است. برای انجام بعضی کارها، DNA به رشته های RNA تبدیل می شود و سپس این مولکولهای RNA، پیغام هایی را به ریبوزوم (مرکز پروتئین سازی سلول) می برند. برای همین این مولکولها را mRNA(messenger RNA) یا RNA پیغام رسان می نامند. در واقع DNA با فرستادن mRNA، فرآیند پروتئین سازی را هدایت می کند.
مقایسه RNA با DNA
RNA و DNA هر دو اسید نوکلئیک هستند، اما در سه چیز تفاوت دارند؛ نخست این که برخلاف DNA که دو رشتهای است، RNA یک مولکول تکرشتهای است و زنجیرهٔ بسیار کوتاه تری از نوکلئوتیدها را دارد. دوم این که در حالی که DNA دارای قند دئوکسیریبوز میباشد، RNA دارای ریبوز است (در دئوکسیریبوز هیچ گروه هیدروکسیلی به حلقه پنتوزی در جایگاه ۲ پیوند ندارد). این گروههای هیدروکسیلی، پایداری RNA را کمتر از پایداری DNA میسازند زیرا داشتن گروه هیدروکسیل ریبوز را برای واکنش آبکافت آمادهتر میسازد. سوم این که برخلاف DNA در RNA، باز تکمیلکنندهٔ آدنین، تیمین نیست بلکه اوراسیل میباشد که شکل متیلینشدهای از تیمین میباشد. بیشتر RNAهای کارا از دیدگاه زیستی که شامل RNA کوچک هستهای، RNA رناتنی، RNA جابجایی، RNA پیامرسان و دیگر RNAهای بیرمز، گه گاه دارای چیدمانهای خود تکمیلکنندهای هستند که به بخش هایی از RNA این اجازه را میدهند که با خودش جفت شده و تا بخورد و مارپیچهای دوتایی را پدید آورند (همانند DNA). برخلاف DNA، ساختار آنها دارای مارپیچهای دوتایی دراز نیستند اما در جای جای آنها گروههایی از مارپیجهای کوتاه دیده میشود.
ساختار
هر نوکلئوتید در آرانای دارای یک قند ریبوز با کربنهای شمارهگذاریشده از ۱ تا ۵ است. یکی از بازهای آدنین، گوانین، سیتوزین، یا اوراسیل به کربن شمارهٔ ۱ پیوند میخورد. به آدنین و گوانین، خانوادهٔ پورینها (دوحلقهایها) گفته میشود و به سیتوزین و اوراسیل، خانوادهٔ پیریمیدینها (تکحلقهایها) گفته میشود. گروههای فسفات دارای یک بار منفی هستند که با پیوند به آرانای، آن را یک مولکول باردار میسازند. بازها ممکن است پیوندهای هیدروژنی میان سیتوزین با گوانین، آدنین با اوراسیل، و گوانین با اوراسیل را تشکیل دهند. به هر حال برهمکنشهای دیگری هم امکانپذیر میباشد، برای نمونه، پیوند یک گروه از بازهای آدنینی به همدیگر در یک برآمدگی یا تترالوپ GNRA که یک جفت باز گوانین–آدنینی دارد. ویژگی ساختاری مهم آرانای که آن را از دیانآ جدا میسازد، داشتن یک گروه هیدروکسیل در کربن شمارهٔ ۲ قند ریبوز است. بودن این گروه به این میانجامد که در شکل هندسی زنجیرهٔ مارپیچی آن با دیانآ تفاوت پیدا کند. دومین نتیجه پیامد داشتن این گروه هیدروکسیل در کربن ۲، در نواحی انعطافپذیری شکلی (تطبیقی) از یک مولکول آرانای است (که در تشکیل یک مارپیچ دوتایی درگیر نیست)، آرانای تنها با چهار باز توصیف میشود که عبارتند از آدنین، سیتوزین، گوانین، و اوراسیل، در آرانای ریبوزومی، بسیاری از اصلاحات پس از رونویسی، در نواحی بسیار عملکردی اتفاق میافتد، از جمله مرکز پپتیدیل ترانسفراز و زیرواحد رابط، که نشاندهندهٔ این است که آنها برای عملکرد عادی، مهم هستند. شکل عملکردی مولکولهای تکرشتهای آرانای، کاملاً مانند پروتئینها، به یک ساختار سوم ویژهای نیاز دارد. چارچوب (داربست) این ساختار توسط عناصر ساختاری دوم تولید میشود که همان پیوندهای هیدروژنی درونمولکولی هستند. این ساختار دوم به پدید آمدن چندین نمایهٔ قابل شناسایی مانند حلقههای سنجاق سری، شکمخوردگیها، و حلقههای درونی میانجامد. از آنجایی که آرانای باردار است، یونهای فلزی از جمله Mg2+ برای پایاسازی بسیاری از ساختارهای دوم و سوم مورد نیاز هستند.
ما درباره صفر مطلق شنیدهاید، تقریبا 273 درجه سانتیگراد زیر صفر. آیا میدانید در این دمای خاص چه اتفاقاتی میافتد؟ چرا دستیابی به این دما هیچ وقت در عمل امکانپذیر نبوده است؟ و چه نقاط یا اجرامی در زمین، یا حتی دنیا وجود دارند که به این دما نزدیکند؟
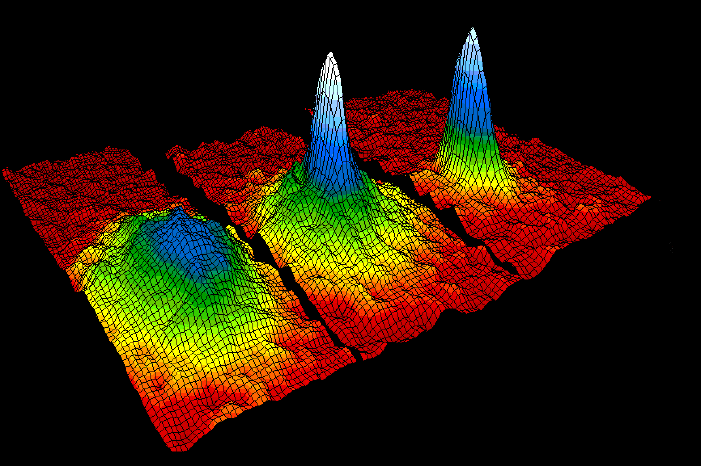 در واقع به نظر میرسد که هنوز هم ما جواب این سوالها را کامل نمیدانیم، زیرا اتفاقاتی که در این دما میافتند، همچنان شگفتانگیز و غافلگیرکننده است. برای نمونه، هفته پیش دانشمندان اعلام کردهاند که مولکولهای گاز بسیار سرد شده میتوانند تا صد بار بیشتر از مولکولهای گاز در دمای اتاق، واکنش شیمیایی داشته باشند.
در واقع به نظر میرسد که هنوز هم ما جواب این سوالها را کامل نمیدانیم، زیرا اتفاقاتی که در این دما میافتند، همچنان شگفتانگیز و غافلگیرکننده است. برای نمونه، هفته پیش دانشمندان اعلام کردهاند که مولکولهای گاز بسیار سرد شده میتوانند تا صد بار بیشتر از مولکولهای گاز در دمای اتاق، واکنش شیمیایی داشته باشند.
به گزارش نیوساینتیست، در آزمایشهایی که در دمای نزدیک به دمای اتاق صورت میگیرند، واکنشهای شیمیایی با کاهش دما کندتر میشوند. اما اخیرا دانشمندان متوجه شدهاند که در دمای نزدیک به صفر مطلق (15/273- سانتیگراد یا صفر درجه کلوین) تبادل اتمها کماکان انجام میگیرد و این امر، باعث ایجاد اتصالات شیمیایی جدید در این فراید میشود. به نظر میرسد این فرایند مدیون تاثیرات خارقالعاده کوانتومی است که قابلیتهای مولکولها را در دمای پایین افزایش میدهد.
به گفته دبورا جین از دانشگاه کلرادو که مقالهای در مورد این یافته جدید منتشر کرده، شاید خیلی منطقی به نظر برسد که انتظار نداشته باشیم در صفر مطلق اثری از واکنشهای شیمیایی باشد، اما در واقع این طور نیست و در این دما واکنشهای فراوانی صورت میگیرد.
اما چرا دست یافتن به دمای صفر مطلق غیرممکن است؟
از نظر عملی، این کار نیاز به این دارد که گرمای گاز را بگیرید؛ اما هر چه دما را پایین بیاورید، گرمای بیشتری را باید از گاز بگیرید. در واقع برای رسیدن به صفر مطلق باید این کار را تا بینهایت ادامه داد. در زبان کوانتوم، باید به سراغ اصل عدم قطعیت هایزنبرگ برویم که میگوید هر چه دقیقتر در مورد سرعت یک ذره بدانیم، کمتر در مورد موقعیت آن خواهیم دانست و برعکس. بنابراین اگر میدانید که اتمهایتان در آزمایشتان وجود دارند، باید تاحدی نسبت به سرعت حرکت آنها و این که بالای صفر مطلق هستند یا نه، نامطمئن باشید، مگر این که وسعت آزمایش شما به اندازه کل هستی باشد!
فکر میکنید سردترین جای منظومه شمسی ما کجاست؟
سردترین جایی که تا به حال در منظومه شمسی ما پیدا شده، روی کره ماه است. سال گذشته، ماهواره اکتشافی ماه ناسا، دمای گودال همیشه در سایهای را در قطب جنوب ماه اندازهگیری کرد: 240- درجه سانتیگراد. این دما حتی از دمای اندازهگیری شده برای پلوتو که فاصلهاش از خورشید 40 برابر فاصله زمین از خورشید است نیز 10 درجه سردتر است.
فکر میکنید سردترین جرم طبیعی دنیا چه چیزی باشد؟
سردترین جای شناخته شده دنیا، قلب سحابی بومرنگ است که در منظومه قنطورس قرار گرفته و پنجهزار سال نوری با ما فاصله دارد. دانشمندان در سال 1997/ 1376 گزارش کردند که گازهای به جا مانده از یک ستاره مرکزی در حال مرگ، با سرعت خبرهکنندهای جارو میشوند و آن ناحیه از فضا تا دمای یک درجه کلوین سرد شده است، یعنی تنها یک درجه گرمتر از دمای صفر مطلق. معمولا آثار به جا مانده از تشعشعات حاصل از انفجار بزرگ، یا همان تابش ریزموج زمینه کیهانی، ابرهای گازی موجود در فضا را تا 2.7 کلوین گرم می کند. اما انبساط سحابی بومرنگ نوعی یخچال کیهانی پدید آورده که باعث میشود گازها سرمای غیرعادی خود را همچنان حفظ کنند و گرمتر از این نشوند. -
این حساب، سردترین جسم موجود در فضا چیست؟
اگر ماهوارههای مصنوعی را هم به حساب بیاورید، هنوز اجرام سردتری هم پیدا میشود. برخی ابزار موجود در تلسکوپ فضایی پلانک متعلق به آژانس فضایی اروپا، که اردیبهشت ماه 1388 به فضا پرتاب شد، تا دمای 0.1 کلوین سرد شدهاند تا پارازیتهای ریزموجی را که ممکن است دید ماهواره را مختل نمایند، متوقف کنند. محیط فضا، در ترکیب با سیستمهای خنککننده مکانیکی و سرمازاهایی که از گازهای هلیوم و هیدروژن استفاده میکردند، طی چهار مرحله متوالی توانستند سردترین جرم فضا را در 0.1 کلوین نگه دارند.
کمترین دمایی که در آزمایشگاهها به آن دست یافتهایم، چه قدر بوده است؟
با همه آنچه گفته شد، رکورد کمترین دما متعلق به یک آزمایشگاه روی سیاره زمین است. در سال 2003/ 1382 دانشمندان موسسه فناوری ماساچوست (ام.آی.تی) اعلام کردند که ابری از اتمهای سدیم را تا 0.45 نانوکلوین سرد کردهاند، که این رقم رکورد را شکست. پیش از آن، در سال 1999/ 1378 دانشمندان دانشگاه صنعتی هلسینکی در کشور فنلاند توانسته بودند قطعهای از فلز رودیم را تا 1 نانوکلوین سرد نمایند. با این وجود، این دما تنها برای نوع خاصی از جنبش (که در کوانتوم چرخش هستهای نامیده میشود) است و نه دمای کلی همه جنبشهای ممکن.
 فکر میکنید گازها در دمای نزدیک به صفر مطلق چه رفتار عجیب و غریبی از خود نشان میدهند؟
فکر میکنید گازها در دمای نزدیک به صفر مطلق چه رفتار عجیب و غریبی از خود نشان میدهند؟
در گازها، مایعات و جامداتی که روزمره با آنها سر و کار داریم، جنبش اتمها و مولکولها و برخورد آنها با یکدیگر باعث گرما یا انرژی حرارتی میشود. اما در دماهای بسیار پایین، چنین نیست. در این دماها، قوانین عجیب مکانیک کوانتوم حاکم است؛ به طوری که مولکولها به روال معمول با یکدیگر برخورد نمیکنند، بلکه امواج مکانیکی کوانتوم آنها گسترش مییابند و با هم همپوشانی پیدا میکنند. وقتی آنها بدین صورت همپوشانی پیدا میکنند، حالت چگالش بوز- انیشتین را شکل میدهند که در آن، اتمها به نحوی رفتار میکنند که انگار یک اَبَراتم واحد هستند. اولین چگالش بوز- انیشتین خالص، در سال 1995/ 1374 در کلرادو با استفاده از ابر اتمهای روبیدیومی ساخته شد که تا دمای کمتر از 170 درجه کلوین سرد شده بودند و پدیدآورندگان آن، توانستند جایزه نوبل فیزیک را از آن خود کنند.
 سردترین نقطه زمین
سردترین نقطه زمین
گاز SF6 در صنعت برق، به عنوان یک ماده عایقی در تجهیزات فشار قوی و در سطوح ولتاژ بالا بسیار کاربرد دارد.اگرچه SF6 خالص به لحاظ شیمیایی خنثی می باشد، اما در عین حال یک گاز گلخانه ای قوی با یک شبکه مولکولی است که خواص آن در شرایط گرما، بسیار فراتر از دی اکسید کربن خواهد بود. ساختمان مولکولی گاز SF6 به صورت یک هشت ضلعی است که در هر گوشه آن یک اتم فلوئور و در مرکز آن یک اتم گوگرد قرار گرفته و فاصله هر اتم از اتم فلوئور 58 آنگستروم است .
وزن اتمی این گاز برابر با 06/146 و در فرمول شیمیایی آن 95/21% گوگرد و 05/78% فلوئور موجود است .در حالت گازی از قانون گازهای طبیعی پیروی میکند و لذا تغییر فشار فقط با تغییر درجه حرارت و آن هم در محدوده به نسبت بزرگی از آن صورت می گیرد . ویژگی فشار- حرارت گاز SF6 نمایانگر حالت تعادل بین گاز و مایع است یعنی در همان حالتی که در سیلندرهای حامل خود وجود دارد.
SF6 یکی از نادرترین عناصر غیر اکتیو در شرایط معمولی است . در یک محفظه کوارتز تا 500 درجه سانتی گراد هیچ تجزیه ای روی آن صورت نمی گیرد . در درجات بالاتر از 150 درجه سانتی گراد بعضی از فلزات به عنوان کاتالیزور در جهت تجزیه حرارتی به تدریج روی آن موثر واقع میشود ، لذا باید در انتخاب یک فلز مناسب جهت محفظه SF6 دقت لازم صورت گیرد . SF6 غیر سمی ، غیر قابل اشتعال و دارای خاصیت خوب حرارتی و انتقال حرارتی ( 6/1 برابر هوا) است .
نمودار این صفحه مربوط به میزان فشار – درجه حرارت گاز SF6 است .
گاز هگزا فلوئورید گوگرد ( SF6) یک دی الکتریک عالی با خواص بی نظیر در قطع کنندگی ( خاموش کردن ) قوس می باشد و این ویژگی منجر به کاربرد وسیع و موفقیت آمیز در کلیدهای قدرت پستهای گازی شده است . معرفی و شناخت آن در سال 1960 بوده و تجهیزات گازی SF6 تا سال 1980 ساخته شده اند . امروزه ، کاربرد این گاز به حد مطلوبی رسیده و تعداد تجهیزات تعویضی ( تجهیزات روغنی جایگزین شده با گازی ) ، افزایش یافته است . تحت شرایط ایده آل ، وقتی یک عمل تخلیه در کلید رخ می دهد ، هرکدام از اتمهای فلوئور موجود در گاز SF6 یک الکترون گرفته و از اتم گوگرد جدا می شوند و هنگام پایان عمل ، آن الکترون بدست آورده را از دست داده و با ترکیب با یک اتم گوگرد ، دوباره گاز SF6 را تشکیل میدهد که به این مراحل “ خودسازی ” و یا “ خواص بازیابی ” گاز SF6 گویند . این واکنش در تجهیزات الکتریکی گازی ( SF6 ) فشار قوی رخ میدهد و وقتی که ذرات دیگری از قبیل اکسیژن ، آب حاصل از آلودگی اتمسفری ، کربن موجود در مؤلفه های تفلونی کلید ، مس ، تنگستن موجود در کنتاکتها و همچنین آلومینیوم ، با ذرات گوناگونی که از تجزیه SF6 بوجود آمده اند برخورد نماید ، واکنش میدهد .
علاوه بر مزایای فوق ، تجهیزات تزریق شده با گاز SF6 ، نیازی به تعمیرات و نگهداری نداشته و بدون دردسر می باشد . شایان توجه اینکه SF6 توانسته استفاده از تجهیزات روغنی را محدود سازد ، از اینرو با توجه به نیاز صنعت ، دستورالعملهای جدید مطابق با آنها ( تجهیزات گازی ) با موارد جدید باید تطابق یابد. ایمنی، نوع عملکرد آنها در خاموش کردن قوس و در نظر گرفتن اثر گلخانه ای محیط زیست این گاز ( عدم تاثیر در سوراخ شدن لایه ازن ) ، از جمله این موارد است که علاوه بر ایجاد تغییر کاربری قدیمی گاز SF6 ، انگیزه زیادی در ارزیابی فرآیند گاز و استفاده مجدد از گازهای ذخیره شده بوجود آورده است .
در استفاده از این گاز ، کاهش هزینه تعمیرات ( به جهت اینکه کلیدهای گازی در مقایسه با دیگر کلیدها ، به تعمیرات کمتری نیاز دارند ) ، امکان مونیتورینگ اجزاء داخلی کلید و کاهش هزینه بازرسی مؤلفه های داخلی کلید، هزینه های راه اندازی در فرایندهای گازی کم می شود ، قابلیت اطمینان بهبود میابد ، ایمنی بالا از جمله مزایای این گاز است .
استحکام الکتریکی SF6 به اضافه خواص بالا کاربرد آن را در برق فشار قوی در دامنه بسیار گسترده ای امکان پذیر ساخته است زیرا استحکام الکتریکی این گاز در فشار یک اتمسفری و در شرایط کاملاً برابر چند برابر استحکام الکتریکی هوا یا ازت است . لذا تقلیل حجم و وزن دستگاههای مورد کاربرد SF6 از یک اندازه حد اقل برخوردار است . به عبارت دیگر ، با در نظر گرفتنن یک فشار برابر برای هوا و SF6 فاصله بین دو نقطه ار سطوح پتانسیل تقلیل پیدا می کند یا با در نظر گرفتن یک استحکام الکتریکی برای این دو فشار مورد نیاز و وزن دستگاه ها کمتر میشود و یا با در نظر گرفتن عایق روغن از نظر کاربرد نه تنها SF6 سبکتر از روغن است بلکه از نظر حجم نیز امکان بکار گیری یک حجم کوچکتر برای SF6 وجود خواهد داشت ; زیرا موقع بروز قوس الکتریکی در محفظه های حاوی SF6 و روغن افزایش فشار در محفظه SF6 فقط به اندازه یک عدد اعشاری خواهد بود حال آنکه فشار تولیدی توسط قوس الکتریکی و احیاناً تجزیه مقدار کمی از روغن سبب افزایش بسیار زیاد فشار محفظه روغن میشود .در کاربرد یک گاز به عنوان ماده عایقی در فشار قوی و قضاوت درباره استحکام الکتریکی آن با استفاده از قانون پاشن ، رابطه بین شکست ولتاژ آن گاز نسبت به حاصلضرب فشار ( در یک درجه حرارت ثابت ) یا چگالی آن را ( برای در نظر گرفتن تمام تغییرات فیزیکی آن در درجات حرارت مختلف ) در فاصله تخلیه ، مبدا قرار میدهند .
Ud = f ( P. a ) or Ud = f (δ . a ) { bar.cm}
اگر چگالی نسبی آن را که نسبت به شرایط عادی محاسبه شده باشد ، در نظر بگیریم خواهیم داشت :
Ud = f (δ . a )
هر گاز دارای یک منحنی خاص خود در این نوع است و برای مقایسه بین گازها از این محنحنی استفاده می کنند . مقدار مینیمم ولتاژ شکست برای SF6 برابر 507 ولت در p.d = 0.00035 {bar.cm} و برای هوا 352 ولت در p.d = 0.00073{bar.cm} است .
نمودار این صفحه مربوط به تغییرات استحکام الکتریکی در رابطه با تغییرات فشار و فاصله تخلیه الکتریکی در گاز SF6 و هوا است .
داشتن خواص عالی گاز SF6 سبب کاربرد آن در بسیاری از تاسیسات برق رسانی ، دستگاههای الکتریکی و دیگر صنایع شده است .در صنعت برق فشار قوی ، خاصیت آتش خاموش کن در کلید های فشار قوی ، خاصیت عایقی آن در پستهای سر بسته گازی از نوع SF6 (GIS) کابلهای SF6 و خطوط لوله انتقال انرژی الکتریکی ، ترانسفورماتورها ، خازنهای اندازه گیری برای ولتاژهای بالا ، ژنراتورهای الکترو استاتیکی ، دستگاههای اشعه ایکس ، برقگیرها و نیز در صنایع ریخته گری ( برای جلوگیری از نفوذ هوا ) و صنایع شیشه سازی استفاده می کنند .خاصیت خنک کنندگی این گاز موجب استفاده از آن در ترانسفورماتورهای قدرت نیز امکان پذیر ساخته است . برخی از کارخانه های ترانسفورماتور سازی ، ترانسفورماتورهای با ولتاژ 66 کیلو ولت و قدرت 20 مگا ولت آمپری ( سیستم خنک کنندگی ONAN و ONAF ) را تولید کرده اند .
علت آزمایش گاز SF6 جهت افزایش ایمنی ، کاهش آثار مخرب زیست محیطی ، صرفه جوئی هزینه تعمیرات و نگهداری روشهای بکارگیری توسعه یافته ( بهینه سازی روشهای کاربرد قدیمی ) است .
تحلیل آلاینده های گاز ، فرایندهای تشخیص ترکیب مواد حاصل از تجزیه ، هنگام قوس الکتریکی و چگونگی انجام آن فرآیندها ، اصول تشخیص شرایط عملکرد تجهیزات گازی SF6 را فراهم می سازد .
حالت نمونه ذیل را ملاحظه فرمائید :
این جدول مربوط به یک کلید 161 کیلوولتی و 2000 آمپری از نوع SF6 تک فشار ، تانک تحت ولتاژ و با مکانیزم عملکرد فنر است که جهت برقراری مدار یک بانک خازنی 168 مگاواری ، 2 تا 3 بار در روز عمل می کند . گازهای نامبرده در این جدول ، گازهائی هستند که هنگام عملکرد یک کلید گازی SF6 ، در محفظه قطع آن کلید متصاعد میشوند . درصد این گازها در هر فاز قابل ملاحظه است . بعنوان مثال، 8/99% از گاز داخل محفظه فاز 1 کلید مورد نظر ، گاز SF6 است ( جمع هر ستون ، مقدار 100000 است ) . در 20 سپتامبر 1997 ، یک واحد توزیع کنترل از راه دور ، این کلید را بکار انداخت . فاز دوم این کلید ، دچار اشکال شد و نتوانست عمل کند و نتیجتا رله جریان زیاد و رله خطای کلید فعال شده و عملکرد این رله ها باعث ایزوله شدن باس سکشن هائی که نقش تغذیه کلید را بعهده داشتند، گردید . پس از این فاصله زمانی مجاز ، مرکز توزیع ( دیسپاچینگ ) قادر به برقدار کردن از راه دور باس سکشن ها، گردید. این شکست تاثیری در گسیختگی این کلید قطع جریان نداشت. کلید از نظر معیوب بودن ، بازبینی شد . فشار گاز در تمام فازها نرمال بود و بعد از آخرین عمل وصل کلید ، فنرها دشارژ شدند . تمامی آزمایش ها ، عایقی ، زمانبندی، عملکردها و مقاومت کنتاکتها با نتایج رضایت بخشی بدست آمد و هیچ مشکلی در کلید مشاهده نشد .
این نمونه های گاز از هر سه فاز جمع آوری شده و مقدار زیاد گاز CF4 در فاز 2 ، بیانگر خوردگی در تفلون است . تصمیم بر این شد که این گاز را از کلید خارج نموده و به صورتیکه قابل مشاهده باشد، کلید را بازرسی کنند . قوس در فاصله میانی محفظه قطع و کنتاکتهای ثابت و متحرک مشاهده شد . یعنی این قوس بین کنتاکتهای ثابت و متحرک صورت نپذیرفته ، از اینرو فاز دوم این کلید تعویض شد ( تا قوس بین محفظه قطع و کنتاکتها زده نشود که این خود ، باعث متصاعد شدن گاز CF4ناخواسته و اضافی در این فاز گردد ) .
روشهای رایج برای بازرسی نشتی SF6 ، شامل استفاده از صابون است که با این عمل، در صورت وجود نشتی، حبابهای گاز در محل نشتی ظاهر می شوند و بدین ترتیب نشتی تشخیص داده می شود. این روش نسبتا" زمان بر بوده و بدلیل اینکه لازم است تا تجهیزات مورد بازرسی بی برق گردند، پر هزینه می باشد.
اخیرا" مؤسسهEPRI برای تشخیص نشتی گاز SF6 ، روش جدیدی مبتنی بر استفاده از دوربین “GasVue”،برای انجام بازرسی در محل تجهیزات ارائه نموده است. دوربین لیزری“GasVue” یک فناوری جدید در بازرسی و آشکار سازی نشتی گاز SF6می باشد. اساس کار این دوربین بر ترکیب Co2laser (قسمتی که طول موجهای مادون قرمز را برای جذب و شناسایی SF6هماهنگ می نماید)با یک سیستم تصویری مادون قرمز می باشد و بدین ترتیب، امکان مشاهده نشتی SF6 که برای چشم غیر مسلح و دیگر تجهیزات بازرسی بصری، غیر محسوس است، فراهم می گردد.
این دوربین با سرعت و دقتی فراوان و بی نیاز از خروج تجهیزات تحت بازرسی از حالت بهره برداری، حتی نشتی ناشی از یک سوراخ ریز را نشان می دهد. استفاده از این دوربین سبب میگردد که شرکتهای برق، نشتی های مربوط به گاز SF6 را سریعتر و صحیحتر از روشهای رایج تشخیص دهند. در نتیجه با استفاده از این سیستم، هزینه های مربوط به عیب یابی کاهش یافته و میزان اتلاف گاز SF6 نیز کمتر می گردد.
بعلاوه می توان نشتی روی سطوحی را که به سختی در دسترس می باشند شناسایی کرد و نیز با توجه به سایر تکنیکها، حتی طیفهای ضعیف گاز و یا نشتیهای پالسی را که در حال خروج هستند، نشان داد. دوربین مذکور، ایمنی عملیات بازرسی را بهبود می بخشد چرا که کاربر دوربین می تواند از یک فاصله امن از تجهیزات و نیز در ارتفاع معینی از زمین که عموما" بر روی نردبانها و چوب بستها می باشد، عمل بازدید را هدایت نماید.
برای آشکار سازی نشتی گاز SF6 در کلیدها و دیگر تجهیزات یک پست در ایالت ایلی نویز( آمریکا) ، بجای آزمایشات مرسوم، از دوربین لیزری“GasVue” استفاده گردید. با صرف نظر از هزینه های مشترک بین این روش و آزمایشهای مرسوم حبابی(صابونی)، برآورد بعمل آمده نشان داد که هزینه صرفه جویی شده به واسطه این روش کاربردی ساده، معادل 12 هزار دلار می باشد. پس از سرمایه گذاری مؤسسه EPRI در امر پیشرفت دوربین مورد نظر، شرکت "ادیسون" در نیویورک، در چند نوبت از ماه، از این دوربین استفاده کرده است.همچنین شرکت برق آفریقای جنوبیEskom از این دوربین در چهار پست خود استفاده کرده است.